- Уравнение состояния Ли — Эрбара — Эдмистера
-
Уравнение состояния Ли — Эрбара — Эдмистера
Уравнение состояния 
Статья является частью серии «Термодинамика». Уравнение состояния идеального газа Уравнение Ван-дер-Ваальса Уравнение Дитеричи Уравнение состояния Редлиха — Квонга Уравнение состояния Барнера — Адлера Уравнение состояния Суги — Лю Уравнение состояния Бенедикта — Вебба — Рубина Уравнение состояния Ли — Эрбара — Эдмистера Разделы термодинамики Начала термодинамики Уравнение состояния Термодинамические величины Термодинамические потенциалы Термодинамические циклы Фазовые переходы править Уравнение состояния Ли — Эрбара — Эдмистера — трёхпараметрическое уравнение состояния углеводородных систем, выведенное[1][2] Ли (B.-I. Lee), Эрбаром (J. H. Erbar) и Эдмистером (W. C. Edmister) в 1972—73 годах. Уравнение разработано таким образом, чтобы определять энтальпии и константы фазового равновесия углеводородных смесей, а не волюметрических свойств. Данное уравнение является улучшением уравнения состояния, полученного[3][4] в 1971 году Ли и Эдмистером.
Уравнение Ли — Эрбара — Эдмистера имеет вид:
где
- a = [(0,246105 + 0,02869ω) − (0,037472 + 0,149687ω)Tr +
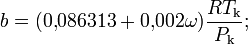
![c=[(0{,}451169+0{,}00948\omega)T^{-1/2}_\mathrm{r}+(0{,}387082+0{,}078842\omega)T^{-2}_\mathrm{r}]\frac{R^2T^2_\mathrm{k}}{P_\mathrm{k}};](http://dic.academic.ru/pictures/wiki/files/51/399af4a8b7fde5ef1a0e43d828f6697c.png)
- P — давление, Па;
- T — абсолютная температура, К;
- V — мольный объём, м³/моль;
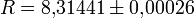 — универсальная газовая постоянная, Дж/(моль·К);
— универсальная газовая постоянная, Дж/(моль·К);- Tk — критическая температура;
- Pk — критическое давление;
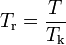 — приведённая температура;
— приведённая температура;- ω — фактор ацентричности (англ.) Питцера.
Литература
- Рид Р., Праусниц Дж., Шервуд Т. Свойства газов и жидкостей: Справочное пособие / Пер. с англ. под ред. Б. И. Соколова. — 3-е изд. — Л.: Химия, 1982. — 592 с.
- Уэйлес С. Фазовые равновесия в химической технологии: В 2-х ч. Ч. 1. — М.: Мир, 1989. — 304 с. — ISBN 5-03-001106-4.
См. также
- Уравнение состояния идеального газа
- Уравнение Ван-дер-Ваальса
- Уравнение Дитеричи
- Уравнение состояния Редлиха — Квонга
- Уравнение состояния Барнера — Адлера
- Уравнение состояния Суги — Лю
- Уравнение состояния Бенедикта — Вебба — Рубина
Примечания
- ↑ Lee B.-I., Erbar J. H., Edmister W. C. // Chemical Engineering Progress. — 1972. — В. 9. — Т. 68. — С. 83.
- ↑ Lee B.-I., Erbar J. H., Edmister W. C. Prediction of thermodynamic properties for low temperature hydrocarbon process calculations // The American Institute of Chemical Engineers Journal. — 1973. — В. 2. — Т. 19. — С. 349—356.
- ↑ Lee B.-I., Edmister W. C. A generalized method for predicting vapor-liquid equilibrium // The American Institute of Chemical Engineers Journal. — 1971. — В. 6. — Т. 17. — С. 1412—1418.
- ↑ Lee B.-I., Edmister W. C. New Three-Parameter Equation of State // Industrial and Engineering Chemistry Fundamentals. — 1971. — В. 1. — Т. 11. — С. 32—35.
Wikimedia Foundation. 2010.
Уравнение состояния Ли — Уравнение состояния Стат … Википедия
Уравнение состояния Бенедикта — Вебба — Рубина — Уравнение состояния Статья является частью серии «Термодинамика». Уравнение состояния идеального газа … Википедия
Уравнение состояния Бенедикта — Уравнение состояния Стат … Википедия
Уравнение состояния Редлиха — Квонга — Уравнение состояния Статья является частью серии «Термодинамика». Уравнение состояния идеального газа … Википедия
Уравнение состояния Суги — Лю — Уравнение состояния Статья является частью серии «Термодинамика». Уравнение состояния идеального газа Уравнен … Википедия
Уравнение состояния Редлиха — Уравнение состояния Стат … Википедия
Уравнение состояния Барнера — Адлера — Уравнение состояния Статья является частью серии «Термодинамика». Уравнение состояния идеального газа … Википедия
Уравнение состояния Барнера — Уравнение состояния Стат … Википедия
Уравнение состояния Суги — Уравнение состояния Статья является час … Википедия
Уравнение состояния идеального газа — Уравнение состояния Стат … Википедия

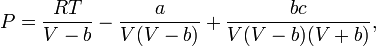
![+(0{,}16406+0,023727\omega)T^{-1}_\mathrm{r}+(0{,}04937+0{,}132433\omega)T^{-2}_\mathrm{r}]\frac{R^2T^2_\mathrm{k}}{P_\mathrm{k}};](http://dic.academic.ru/pictures/wiki/files/100/d3ce1fa2b3ffc131f462fa0386332525.png)