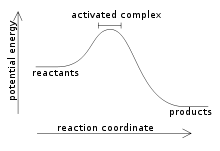
- Экзотермические реакции
-
Экзотермическая реакция — химическая реакция, сопровождающаяся выделением теплоты. Противоположна эндотермической реакции.
Полное количество энергии в химической системе чрезвычайно трудно измерить или подсчитать. С другой стороны, изменение энтальпии ΔH в химической реакции гораздо легче измерить или сосчитать. Для этих целей используют калориметры. Измеренное значение ΔH соотносится с энергией связи молекул следующим образом:
ΔH = энергия, потраченная на разрыв связей (Энергия разрыва химической связи)— энергия, выделенная при образовании связей продуктов реакции.
Для экзотермических реакций эта формула даёт отрицательное значение для ΔH, так как большее значение вычитается из меньшего значения. При сгорании водорода, например:
2H2 + O2 → 2 H2O
изменение энтальпии равно ΔH = −483.6 кДж на один моль O2.
Примеры
- Горение топлива в кислороде воздуха.
- Горение пороха.
- Добавление концентрированной серной кислоты в воду.
- Окисление жиров и углеводов в живых организмах.
- Адиабатическое горение
См. также
- Эндотермическая реакция
- Экзотермическое превращение // Энциклопедический словарь Брокгауза и Ефрона: В 86 томах (82 т. и 4 доп.). — СПб., 1890—1907.
 Категория:
Категория:- Общая химия
Wikimedia Foundation. 2010.