- Карбид циркония
-
Карбид циркония 
Общие Систематическое наименование монокарбид циркония Традиционные названия карбид циркония Химическая формула ZrC Физические свойства Состояние (ст. усл.) твёрдое Молярная масса 103,23 г/моль Плотность 6,73 г/см³ Термические свойства Температура плавления 3530 °C Температура кипения 5100 °C Теплопроводность (ст. усл.) 11,6 Вт/(м·K) Классификация Рег. номер CAS 12070-14-3 Карби́д цирко́ния – химическое соединение металла циркония и углерода с формулой ZrC. Представляет собой фазу внедрения с широкой областью гомогенности, которая составляет от 38,4 до 50 ат. % углерода, что отвевает формуле ZrC0,62 и ZrC1,0 соответственно[1].
Содержание
Физические свойства
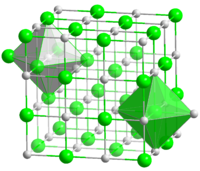
Карбид циркония представляет собой порошок серого цвета. Имеет кубическую гранецентрированную решетку типа NaCl, пространственная группа Fm3m, с периодом а = 0,4693 нм.
- Удельное электрическое сопротивление 50 мкОм∙см
- Коэффициент линейного теплового расширения 7,01∙10-6 1/K (25-1000 °C)
- Микротвёрдость 28,44 ГПа
- Модуль упругости 412 ГПа[2]
Получение
Карбид циркония можно получить одним из следующих способов[3].
- Непосредственным насыщением циркония углеродом:
- Процесс ведут в вакууме, а исходные компоненты берут в виде порошков;
- Восстановлением оксида циркония углеродом с последующим образованием карбида:
- Процесс идет через образование низших окислов циркония и последующего образования карбида циркония по реакции:
- ZrO + C = ZrC + CO
- Этот метод применяется для получения технически чистого карбида циркония в промышленных масштабах. Обычно процесс проводят при температуре около 2000 °C;
- Осаждением из газовой фазы:
- В основе метода лежит реакция:

- Осаждение происходит на поверхности вольфрамовой нити разогретой до температуры 1700-2400 °C. Проведение процесса при высокой температуре (около 2400 °C) позволяет получить монокристаллический осадок. Так же метан может быть заменен толуолом, бензолом или ацетиленом.
Химические свойства
Карбид циркония является химически стойким соединением при комнатной температуре по отношению к серной, соляной, фосфорной, хлорной, щавелевой кислотам и смесям серной и фосфорной, серной и щавелевой кислот. Не растворяется в 10% и 20% растворах гидроксида натрия. Растворяется в кипящих серной, азотной, хлорной кислотах. Сильно растворяется в царской водке, смесях серной и азотной, азотной и плавиковой кислот[3]. Начиная с 700 °C, карбид циркония взаимодействует с кислородом с образованием ZrO2. При высоких температурах, в присутствии азота, образуются карбонитриды циркония.
Применение
Высокая температура плавления и малое поперечное сечение захвата нейтронов карбида циркония позволяет применять его как защитное покрытие на графитовых матрицах в твэлах содержащих карбиды урана и тория. Покрытие из карбида циркония, нанесенное CVD-процессом на диоксид урана, используется как диффузионный барьер от продуктов реакции полураспада ядерного топлива[4]. Композит ZrC-UC используют в термоэлектрогенераторах. Также карбид циркония применяется как абразивный материал для полировки металлов[3].
Примечания
- ↑ Самсонов Г. В. Физическое материаловедение карбидов. — Наукова думка, 1974. — С. 107-109. — 454 с.
- ↑ Самсонов Г. В., Виницкий И. М. Тугоплавкие соединения (справочник). — Металлургия, 1976. — С. 560.
- ↑ 1 2 3 Косолапова Т. Я. Карбиды. — Металлургия, 1968. — С. 300.
- ↑ Effect of Use of Zirconium Carbide Coatings on the VHTR Core Nuclear Design
Соединения цирконияБромид циркония(II) (ZrBr2) • Бромид циркония(III) (ZrBr3) • Бромид циркония(IV) (ZrBr4) • Вольфрамат циркония (Zr(WO4)2) • Гидрид циркония(II) (ZrH2) • Гидрид циркония(IV) (ZrH4) • Гидрид циркония (ZrHx) • Диборид циркония (ZrB2) • Дигидроксид-оксид циркония (ZrО(OH)2) • Дифосфид циркония (ZrP2) • Иодид циркония(III) (ZrI3) • Иодид циркония(IV) (ZrI4) • Карбид циркония (ZrC) • Нитрат циркония(IV) (Zr(NO3)4) • Нитрид циркония(II) (Zr3N2) • Нитрид циркония(III) (ZrN) • Нитрид циркония(IV) (Zr3N4) • Оксид циркония(IV) (ZrO2) • Оксид-дихлорид циркония (ZrOCl2) • Ортосиликат циркония(IV) (ZrSiO4) • Ортоциркониевая кислота (H4ZrO4) • Силицид циркония (ZrSi2) • Сульфат циркония(IV) (Zr(SO4)2) • Сульфид циркония(IV) (ZrS2) • Теллурид циркония(IV) (ZrTe2) • Фосфид циркония (ZrP) • Фторид циркония(II) (ZrF2) • Фторид циркония(III) (ZrF3) • Фторид циркония(IV) (ZrF4) • Хлорид циркония(II) (ZrCl2) • Хлорид циркония(III) (ZrCl3) • Хлорид циркония(IV) (ZrCl4)
Категории:- Соединения циркония
- Карбиды
- Неорганические вещества
- Бинарные соединения
Wikimedia Foundation. 2010.
