- Озоносфера
-
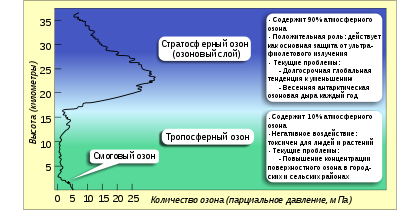 Озоновый слой в атмосфере
Озоновый слой в атмосфере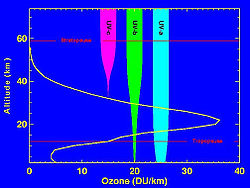 Абсорбция ультрафиолетового излучения озоновым слоем
Абсорбция ультрафиолетового излучения озоновым слоемОзо́новый слой — часть стратосферы на высоте от 12 до 50 км, в котором под воздействием ультрафиолетового излучения Солнца кислород (О2) ионизируется, приобретая третий атом кислорода, и получается озон (О3). Относительно высокая концентрация озона (около 8 мл/м³) поглощает опасные ультрафиолетовые лучи и защищает всё живущее на суше от губительного излучения. Более того, если бы не озоновый слой, то жизнь не смогла бы вообще выбраться из океанов[1] и высокоразвитые формы жизни типа млекопитающих, включая человека, не возникли бы. Наибольшая плотность озона встречается на высоте 20 км, наибольшая часть в общем объёме — на высоте 40 км. Если бы можно было извлечь весь озон, находящийся в атмосфере, и сжать под нормальным давлением, то в результате вышел бы слой, покрывающий поверхность Земли толщиной всего 3 мм. Для сравнения, вся сжатая под нормальным давлением атмосфера составляла бы слой в 8 км.
Содержание
Механизм Чэпмана
Механизм образования, а также расходования озона, был предложен Сиднеем Чэпманом в 1930 году и носит его имя.
Реакции образования озона:
О2 + hν → 2О
О2 + O → О3
Фотолиз молекулярного кислорода происходит в стратосфере под воздействием ультрафиолетового излучения с длиной волны 175—200 нм и до 242 нм.
Озон расходуется в реакциях фотолиза и взаимодействия с атомарным кислородом:
О3 + hν → О2 + О
О3 + O → 2О2
Пути гибели озона
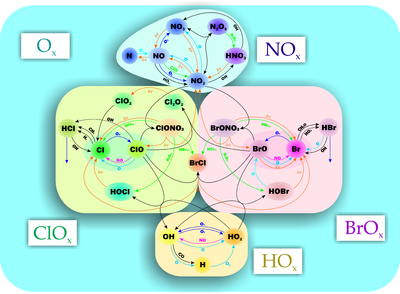 Стратосферная химия озона
Стратосферная химия озонаКроме реакций, входящих в механизм Чэпмана, имеется целый ряд других реакций, приводящих к гибели озона. Их все объединяют в несколько семейств, главными из которых является азотное, кислородное (из механизма Чэпмана), водородное и галогеновое. Эти реакции представляют собой каталитические циклы, поэтому их также называют соответствующими циклами.
Азотный цикл (NOx):
N2O + O(1D) → NO + NO
О3 + NO → NO2 + О2
NO2 + О → NO + О2Водородный цикл (HOx) :
Н2O + O → OH + OH
ОН + О3 → НО2 + О2
НО2 + О3 →ОН + 2О2Хлорный цикл (ClOx):
CFCl3 + hν → CFCl2 + Cl
Cl + O3 → ClO + O2
ClO + O → Cl + O2Доля в расходовании озона различных химических семейств:[2]
Давление, гПа азотное кислородное водородное галогеновое 1.31 0.10 0.26 0.41 0.21 3.78 0.50 0.14 0.11 0.25 8.93 0.68 0.11 0.08 0.13 21.9 0.46 0.12 0.19 0.20 55.8 0.12 0.03 0.48 0.14 Деятельность человека во многом увеличила долю галогенового пути распада стратосферного озона, что привело к возникновению озоновых дыр.
История открытия озонового слоя
Открывателями озонового слоя были французские физики Шарль Фабри и Анри Буиссон. В 1913 году им удалось с помощью спектроскопических измерений ультрафиолетового излучения доказать существование озона в отдалённых от Земли слоях атмосферы.
Интересные факты
Генеральная ассамблея ООН в 1994 году провозгласила ежегодный Международный день охраны озонового слоя.
Тропосфера | Стратосфера | Мезосфера | Термосфера | Экзосфера
Тропопауза | Стратопауза | Мезопауза | Экзобаза
Озоновый слой | Турбопауза | Ионосфера
Ссылки
- ↑ И.К. Ларин Химия озонового слоя и жизнь на Земле // Химия и жизнь - XXI век. — 2000. — № 7. — С. 10–15..
- ↑ Andrew Dessler. The Chemistry and Physics of Stratospheric Ozone. Academic Press. 2000
- Состояние озонового слоя над Россией и прилегающими территориями
- Озоновый слой Земли.
- Химия озонового слоя.
Статьи и обзоры
- Озон в атмосфере. Озоновый слой - ультрафиолетовый щит Земли
- Химия и алхимия озонового слоя
- Охрана озонового слоя в мире
Международные соглашения
- Венская конвенция об охране озонового слоя
- Монреальский протокол по веществам, разрушающим озоновый слой
Wikimedia Foundation. 2010.
