- Оксид калия
-
Оксид калия 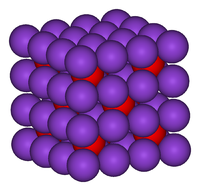
Общие Химическая формула K2O Физические свойства Состояние (ст. усл.) твёрдое Молярная масса 94.20 г/моль Плотность 2.35 г/см³ Термические свойства Температура плавления 740 °C Классификация Рег. номер CAS 12136-45-7 Содержание
Физические свойства
Оксид калия K2O — бледно-жёлтое, иногда бесцветное, редко встречающееся вещество. Содержится в некоторых видах удобрений и цемента.
Химические свойства
Химически активное вещество. На воздухе расплывается, поглощает СО2, давая К2СО3. Бурно реагирует с водой, образуя KOH. Реагирует со спиртом, с эфиром. Энергично взаимодействует с галогенами, расплавленной серой, разбавленными кислотами, образуя различные соединения калия.[1].
Производство
Оксид калия производят взаимодействием кислорода и калия, в результате реакции образуется пероксид калия, K2O2. Обогащением пероксида калием получают оксид:[2]
- K2O2 + 2 K → 2 K2O
Более удобным способом является нагревание нитрата калия с металлическим калием:
- 2 KNO3 + 10 K → 6 K2O + N2
Гидроксид калия не может быть обезвожен до оксида.
См. также
Ссылки
- ↑ Большая Советская Энциклопедия
- ↑ Holleman, A. F.; Wiberg, E. «Inorganic Chemistry» Academic Press: San Diego, 2001. ISBN 0-12-352651-5.
Категории:- Соединения калия
- Основные оксиды
- Твёрдое тело
Wikimedia Foundation. 2010.
