- Оксид хлора(IV)
-
Оксид хлора(IV) 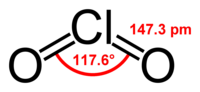
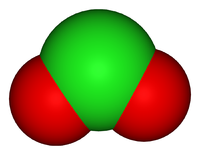
Общие Систематическое наименование Оксид хлора(IV) Химическая формула ClO2 Отн. молек. масса 67,45 а. е. м. Молярная масса 67,45 г/моль Физические свойства Состояние (ст. усл.) газ Термические свойства Температура плавления −59 °C Температура кипения 9,7 °C Энтальпия образования (ст. усл.) +104,60 кДж/моль Классификация Рег. номер CAS 10049-04-4 Рег. номер EINECS 233-162-8 Диоксид хлора ClO2.
Содержание
Физические свойства диоксида хлора
ClO2 — газ красновато-жёлтого цвета, с характерным запахом. При температурах ниже 10 °C ClO2 представляет собой жидкость красно-коричневого цвета. Малоустойчив, взрывается на свету, при контактах с окислителями и при нагревании. Хорошо растворим в воде. Теплота испарения диоксида хлора 6,3 ± 0,1 ккал/моль, критическая температура 192 °C, критическое давление 85 атм. Плотность ClO2 уменьшается от 1,973 г/см³ при −60 °C до 1,653 г/см³ при 5 °C. Диоксид хлора растворим в воде, уксусной и серной кислотах, в четырёххлористом углероде, ацетонитриле, а также в ряде других органических растворителей. Растворимость диоксида хлора возрастает с ростом полярности растворителя. Потенциал ионизации диоксида хлора равен 10,33 ± 0,02 эВ, сродство к электрону 2,378 ± 0,006 эВ. Потенциал окисления-восстановления в водном растворе — E(ClO2/ClO2−) = 0,94 В.
Оксид хлора(IV) имеет нечётное количество электронов (33) и является стабильным радикалом, не проявляющим при нормальных условиях тенденции к димеризации. В газовой фазе ЭПР спектр ClO2 не наблюдается, что объясняется большим числом вращательных уровней его молекулы. ЭПР-спектр раствора оксида хлора(IV) представляет собой широкий синглет, но при некоторых условиях (например, низких температурах) спектральная линия усложняется, превращаясь в широкий квартет вследствие сверхтонкого расщепления на ядрах хлора 35Cl и 37Cl, для которых константы сверхтонкой структуры равны 1,70 ± 0,03 и 1,37 ± 0,03 мT соответственно.
Получение
В лаборатории получают по реакции:
2KClO3 + H2C2O4 → K2CO3 + 2ClO2↑ + CO2↑ + H2O.
Из-за взрывоопасности диоксид хлора невозможно хранить в виде жидкости. Однако адсорбирование на поверхности силикагеля позволяет хранить диоксид хлора при пониженной температуре достаточно долго, а также избавиться от примесей хлора, силикагелем не поглощающегося.
Промышленный метод получения ClO2 основан на реакции:
2NaClO3 + SO2 + H2SO4 → 2NaHSO4 + 2ClO2↑.
Свойства
Кислотный оксид. При растворении в воде образуются хлористая и хлорноватая кислоты (реакция диспропорционирования). Разбавленные растворы устойчивы в темноте, на свету медленно разлагаются:
- 2ClO2 + H2O → HClO2 + HClO3.
Образующаяся хлористая кислота очень неустойчива и разлагается:
- 5HClO2 → 3HClO3 + Cl2↑ + H2O.
ClO2 реагирует со многими с органическими соединенями и выступает окислителем средней силы. Большинство реакций с участием ClO2 протекают по механизму одноэлектронного окисления с образованием органических катион-радикалов и хлорит-иона на первой стадии реакции, но возможно протекание и других реакций, в частности, отрыва атома водорода.
Применение
Используется в основном для отбеливания например, целлюлозы, бумаги, муки и т. п., дезинфекции и стерилизации различных материалов.
Физиологическое действие
Категории:- Оксиды хлора
- Газы
- Отбеливающие вещества
Wikimedia Foundation. 2010.

