- Оксид олова(IV)
-
Оксид олова(IV) 
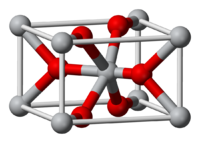
Общие Систематическое наименование Оксид олова Традиционные названия Окись олова Химическая формула SnO2 Физические свойства Состояние (ст. усл.) белые кристаллы Молярная масса 150,71 г/моль Плотность 6,95; 7,0096; 7,036 г/см³ Термические свойства Температура плавления 1127; 1625; 1630 °C Температура кипения 2500 °C Молярная теплоёмкость (ст. усл.) 53,2 Дж/(моль·К) Энтальпия образования (ст. усл.) -577,63 кДж/моль Классификация Рег. номер CAS 18282-10-5 Регистрационный номер EC 242-159-0 RTECS XQ4000000 Оксид олова(IV) — бинарное неорганическое соединение, оксид металла олова с формулой SnO2, белые кристаллы, нерастворимые в воде.
Содержание
Получение
- В природе встречается минерал касситерит — SnO2 с различными примесями.
- Окисление кислородом воздуха монооксид олова:
- Диспропорционирование при нагревании монооксид олова:
- Окисление олова горячей концентрированной азотной кислотой:
- Разложение сульфата олова нагреванием:
- или разбавленной щёлочью:
Физические свойства
Молярная масса 151 кг/кмоль
Оксид олова(IV) из раствора выделяется в виде гидрата SnO2•n H2O (1<n<2, α-модификация). При стоянии переходит химически пассивную β-модификацию (n<1). Соединения стехиометрического состава не выделены. В воде практически нерастворимо, рПР = 57,32
При высушивании гидрата образуется аморфный белый порошок (плотность 7,036 г/см³), который при нагревании переходит в кристаллическую модификацию (плотность 6,95 г/см³).
Оксид олова(IV) образует прозрачные кристаллы тетрагональной сингонии, пространственная группа P 4/mnm, параметры ячейки a = 0,4718 нм, c = 0,3161 нм, Z = 2.
Является полупроводником n-типа.
Химические свойства
- Гидратированная форма переходит в кристаллическую при нагревании:
- Растворяется в концентрированных кислотах:
- При нагревании растворяется в разбавленных кислотах:
- Растворяется в растворах концентрированных щелочей:
- При сплавлении с щелочами образует метастаннаты:
- а с оксидами щелочных металлов образует ортостаннаты:
Применение
- В качестве катализатора.
- Пигмент в керамической глазури.
- При производстве термически и химически стойких стёкол.
- Составляющее прозрачной плёнки-проводника в резистивных сенсорных экранах
Литература
- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0
- Рипан Р., Четяну И. Неорганическая химия. Химия металлов. — М.: Мир, 1971. — Т. 1. — 561 с.
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1992. — Т. 3. — 639 с. — ISBN 5-82270-039-8
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 2-е изд., испр. — М.-Л.: Химия, 1966. — Т. 1. — 1072 с.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
Соединения оловаАцетат олова (Sn(OCOCH3)2) • Бромид олова(II) (SnBr2) • Бромид олова(IV) (SnBr4) • Гексагидроксостаннат(IV) натрия (Na2[Sn(OH)6]) • Гексафенилолово (Sn2(C6H5)6) • Гексахлоростаннат(IV) аммония ((NH4)2[SnCl6]) • Гексахлоростаннат(IV) водорода (H2[SnCl6]) • Гексахлоростаннат(IV) калия (K2[SnCl6]) • Гексахлоростаннаты • Гидроксид олова(II) (Sn(OH)2) • Гидрофосфат олова (Sn(H2PO4)2) • Дифенилолово (Sn(C6H5)2) • Диэтилолово (Sn(C2H5)2) • Иодид олова(II) (SnI2) • Иодид олова(IV) (SnI4) • Нитрат олова(II) (Sn(NO3)2) • Нитрат олова(IV) (Sn(NO3)4) • Оксалат олова (SnC2O4) • Оксид олова(II) (SnO) • Оксид олова(IV) (SnO2) • Перхлорат олова (Sn(ClO4)2) • Пирофосфат олова (Sn2P2O7) • Селенид олова(II) (SnSe) • Селенид олова(IV) (SnSe2) • Станнан (SnH4) • Станнин (Cu2FeSnS4) • Сульфат олова(II) (SnSO4) • Сульфат олова(IV) (Sn(SO4)2) • Сульфид олова(II) (SnS) • Сульфид олова(IV) (SnS2) • Теллурид олова (SnTe) • Фосфат олова(II) (Sn3(PO4)2) • Фторид олова(II) (SnF2) • Фторид олова(IV) (SnF4) • Хлорид олова(II) (SnCl2) • Хлорид олова(IV) (SnCl4)
 Категории:
Категории:- Соединения олова
- Оксиды
- Амфотерные оксиды
Wikimedia Foundation. 2010.








![\mathsf{SnO_2 + 6HCl \ \xrightarrow{}\ H_2[SnCl_6] + 2H_2O }](5a5a2a68259eda26e96a5400109b312b.png)

![\mathsf{SnO_2 + 2NaOH + 2H_2O \ \xrightarrow{60-70^oC}\ Na_2[Sn(OH)_6] }](cdfdab2385fab0dacdbc147d48d29eba.png)



