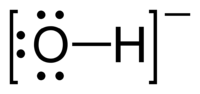- Гидроксид-ион
-
Гидроксид-ион (гидроксид-анион, гидроксильный ион) — отрицательно заряженный ион гидроксила OH−.
Гидроксид-ион изолированно существует в газовой фазе, находится в кристаллической решётке гидроксидов и основных солей, образуется в водных растворах в результате электролитической диссоциации воды или/и растворённых гидроксидов.
Наличие в водном растворе иона OH− в концентрациях, превышающих 10−7 моль/литр приводит к щелочной реакции раствора.
В реакциях комплексообразования гидроксид-ион может выступать в роли лиганда [1].
Рыхлая слоистая кристаллическая структура гидроксидов является следствием высокой поляризуемости и большого ионного радиуса гидроксид-аниона.
Содержание
Ионные равновесия в газовой фазе
В газовой фазе имеет место равновесная реакция

Характеризующая термическую устойчивость гидроксид-иона.
Зависимость константы равновесия (Kp) от абсолютной температуры (T)[2]:
Т,к 1000 2000 3000 4000 5000 6000 Кр 1,66 · 10-7 2,34 · 10-2 1,94 2,23 · 10 1,11 · 102 3,56 · 102 Электролитическая диссоциация оснований
При электролитической диссоциации оснований образуются катионы металла и общие для всех оснований ионы гидроксида:


Таким образом, основания можно определить как химические соединения, дающие в водном растворе гидроксид-ионы.
Электролитическая диссоциация оснований характеризуется константой диссоциации в водных растворах (Кв)[3]:
Основание LiOH NaOH Ca(OH)2 Sr(OH)2 Ba(OH)2 NH4OH Кв, при 25° C 6,75 · 10-1 5,9 4,3 · 10-2 1,5 · 10-1 2,3 · 10-1 1,79 · 10-5 Химические свойства гидроксид-иона
Основной реакцией, в которой принимает участие гидроксид-ион, является реакция нейтрализации кислот и оснований

Которая представляется на ионном уровне:


Последнее выражение представляет собой общее уравнение реакций нейтрализации и показывает, что во всех случаях, когда ионы H+ встречаются с ионами гидроксида OH-, они соединяются в почти недиссоциированные молекулы воды. В реакции гидроксид-ион проявляет свойста нуклеофила – электроизбыточного химического реагента, способного взаимодействовать с электрофилами (электронодефицитными соединениями) по донорно-акцепторному механизму, приводящему к образованию ковалентной химической связи.
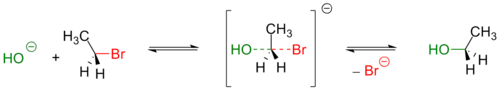
Гидроксид-ион принимает участие в реакциях биомолекулярного нуклеофильного замещения. Например, атом кислорода гидроксид-иона донирует пару электронов на связывание с атомом углерода в молекуле бромэтана:
Типовые реакции нуклеофильного замещения:
 (Образование спиртов)
(Образование спиртов) (Образование кетонов)
(Образование кетонов) (Образование альдегидов)
(Образование альдегидов) (Образование кислот)
(Образование кислот) (Омыление сложных эфиров)
(Омыление сложных эфиров)Примечания
- ↑ Лидин Р.А., Андреева Л.Л., Молочко В.А. Константы неорганических веществ: справочник. — М: Дрофа, 2006. — С. 595-596.
- ↑ Справочник химика. — 2-е изд., перераб. и доп.. — М.-Л.: «Химия», 1964. — Т. 3. — С. 75. — 1008 с.
- ↑ Справочник химика. — 2-е изд., перераб. и доп.. — М.-Л.: «Химия», 1964. — Т. 3. — С. 81. — 1008 с.

См.также
- Нуклеофильное замещение
- Нуклеофил
Источники
- Химическая энциклопедия под ред. И.Л. Кнунянца. — М.: Советская энциклопедия, 1988. — Т. 1.
Категория:- Анионы
Wikimedia Foundation. 2010.